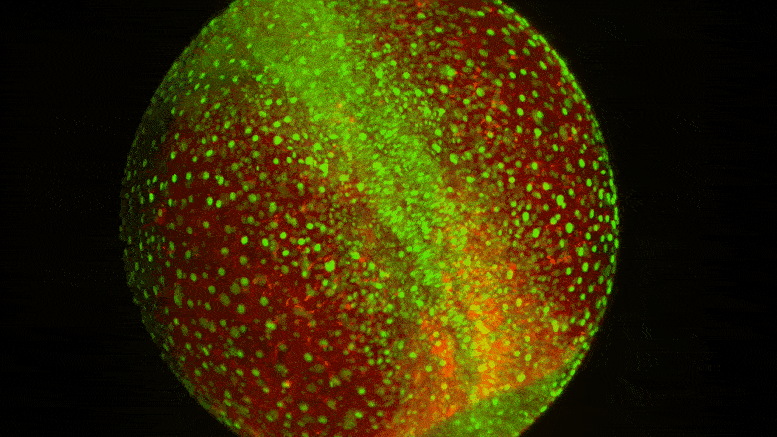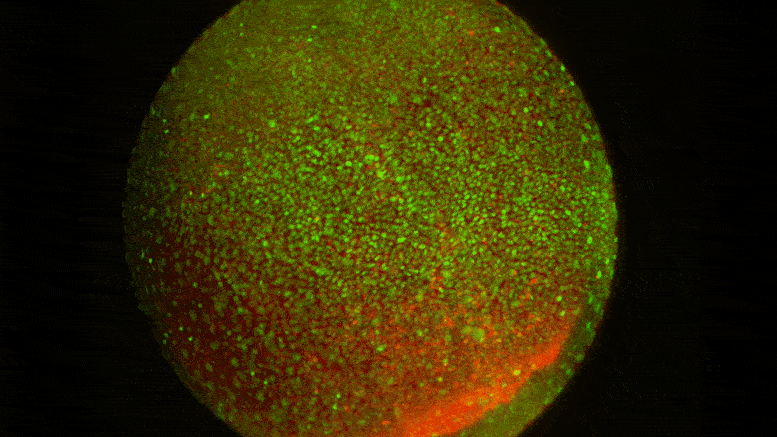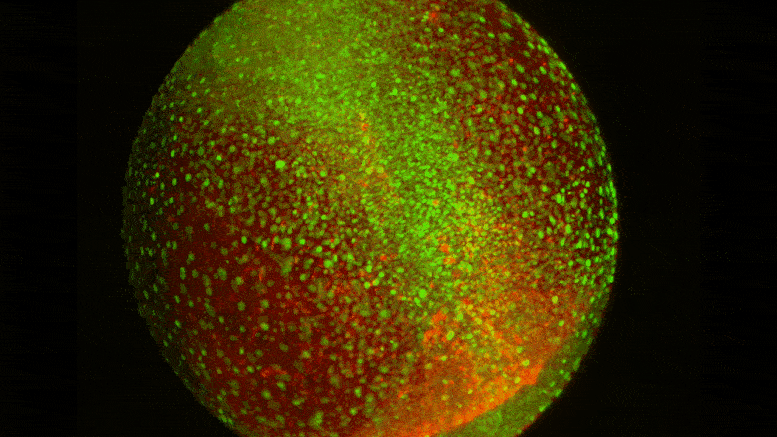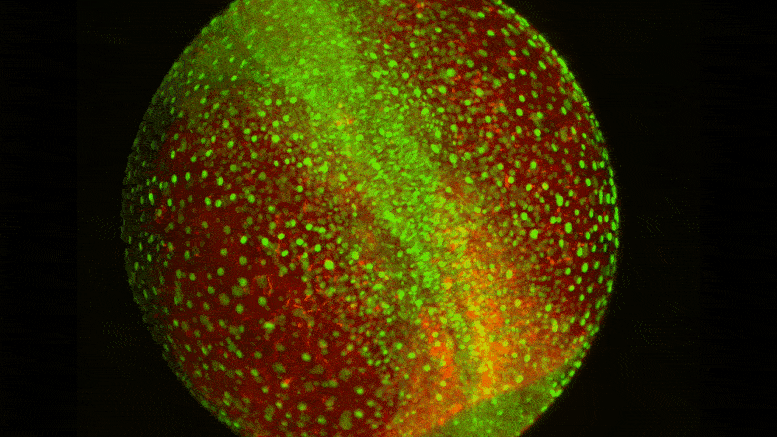
Визуализация живых клеток показывает динамическую среду и степень движения клеток, которое происходит, когда формирующийся спинной мозг формируется на раннем этапе развития. Предоставлено: Тони Цай / Шон Мегасон / Гарвардская медицинская школа.
Ключевой механизм контроля позволяет клеткам формировать ткани и анатомические структуры в развивающемся эмбрионе.
Под микроскопом первые несколько часов жизни каждого многоклеточного организма кажутся нелепо хаотичными. После оплодотворения некогда спокойное одноклеточное яйцо делится снова и снова, быстро превращаясь в визуально шумную мошпаду из клеток, пытающихся занять свое место внутри быстро растущего эмбриона.
Тем не менее, в этом явном пандемониуме клетки начинают самоорганизовываться. Вскоре появляются пространственные структуры, служащие основой для построения тканей, органов и сложных анатомических структур от мозга до пальцев ног и всего, что между ними. На протяжении десятилетий ученые интенсивно изучали этот процесс, называемый морфогенезом, но во многих отношениях он остается загадочным.
Теперь исследователи из Гарвардской медицинской школы и Института науки и технологий (IST) в Австрии обнаружили ключевой механизм контроля, который клетки используют для самоорганизации на раннем этапе эмбрионального развития. Результаты, опубликованные в Наука 2 октября 2020 года пролили свет на процесс, лежащий в основе многоклеточной жизни, и открыли новые возможности для улучшения стратегий тканевой и органной инженерии.
Изучая формирование спинного мозга у эмбрионов рыбок данио, команда под руководством Шона Мегасона, профессора системной биологии в Институте Блаватника в HMS, показала, что разные типы клеток экспрессируют уникальные комбинации молекул адгезии для самосортировки во время морфогенеза. Эти «коды адгезии» определяют, какие клетки предпочитают оставаться связанными и насколько сильно они это делают, даже если в развивающемся эмбрионе происходят широко распространенные клеточные перестройки.
С помощью микропипетки измеряется сила адгезии между двумя клетками. Предоставлено: Тони Цай / Шон Мегасон / Гарвардская медицинская школа.
Исследователи обнаружили, что коды адгезии регулируются морфогенами, главными сигнальными молекулами, которые, как давно известно, управляют судьбой клеток и формированием паттернов в развитии. Результаты предполагают, что взаимодействие морфогенов и адгезионных свойств позволяет клеткам организовываться с точностью и согласованностью, необходимой для построения организма.
«Цель моей лаборатории – понять основные принципы построения биологических форм», – сказал Мегасон, соавтор исследования. «Наши результаты представляют собой новый подход к вопросу морфогенеза, который является одним из старейших и наиболее важных в эмбриологии. Мы видим в этом верхушку айсберга для таких усилий ».
По словам авторов, понимание того, как клетки самоорганизуются на раннем этапе развития, также может помочь усилиям по созданию тканей и органов для клинического использования, такого как трансплантация.
«Создание искусственных тканей для исследований или медицинских применений – критически важная цель, но в настоящее время одна из самых больших проблем – непоследовательность», – сказал ведущий автор исследования Тони Цай, научный сотрудник по системной биологии в Институте Блаватника. «Из понимания и обратной инженерии можно извлечь ясный урок, как клетки развивающегося эмбриона могут строить компоненты организма таким надежным и воспроизводимым способом».
Перетягивание каната
Возглавляемая Цаем и в сотрудничестве с Карлом-Филиппом Гейзенбергом и коллегами из IST Austria, исследовательская группа сначала рассмотрела одну из наиболее устоявшихся рамок морфогенеза, модель французского флага.
В этой модели морфогены высвобождаются из локализованных источников в эмбрионе, подвергая близлежащие клетки воздействию более высоких уровней сигнальной молекулы, чем клетки дальше. Количество морфогена, которому подвергается клетка, активирует различные клеточные программы, особенно те, которые определяют судьбу клетки. Таким образом, градиенты концентрации морфогенов «рисуют» узоры на группах клеток, вызывая воспоминания о различных цветовых полосах французского флага.
Однако у этой модели есть ограничения. Предыдущие исследования лаборатории Megason использовали визуализацию живых клеток и отслеживание отдельных клеток у целых эмбрионов рыбок данио, чтобы показать, что сигналы морфогенов могут быть зашумленными и неточными, особенно на границах «флага». Кроме того, клетки развивающегося эмбриона постоянно делятся и находятся в движении, что может искажать сигнал морфогена. Это приводит к начальному смешанному паттерну типов клеток.
Тем не менее, клетки самоорганизуются в точные шаблоны, даже при шумном начале, и в текущем исследовании команда намеревалась понять, как это сделать. Они сосредоточились на гипотезе, предложенной более 50 лет назад, известной как дифференциальная адгезия. Эта модель предполагает, что клетки прикрепляются к определенным другим типам клеток, самосортировавшись, подобно тому, как масло и уксус разделяются с течением времени. Но было мало доказательств того, что это играет роль в формировании паттерна.
Для исследования Мегасон, Цай и его коллеги разработали метод измерения силы сцепления клеток друг с другом. Они поместили две отдельные ячейки вместе, а затем потянули за каждую ячейку с точно контролируемым давлением всасывания из двух микропипеток. Это позволило исследователям измерить точное количество силы, необходимой для разрыва клеток. Анализируя сразу три клетки, они также могли установить предпочтения в отношении адгезии.
Команда использовала эту технику для изучения формирования паттерна трех разных типов нервных клеток-предшественников, участвующих в построении зарождающегося спинного мозга у эмбрионов рыбок данио.
Эксперименты показали, что клетки одного и того же типа прочно и предпочтительно сцепляются друг с другом. Чтобы идентифицировать соответствующие гены, кодирующие молекулы адгезии, исследователи проанализировали профиль экспрессии генов каждого типа клеток с использованием одноклеточных РНК последовательность действий. Затем они использовали CRISPR-Cas9, чтобы блокировать экспрессию генов-кандидатов по одному. Если формирование рисунка нарушалось, они применяли метод вытягивания, чтобы увидеть, насколько молекула способствует адгезии.
Код адгезии
Три гена – N-кадгерин, кадгерин 11 и протоколадгерин 19 – оказались важными для нормального формирования паттерна. Экспрессия различных комбинаций и разных уровней этих генов была ответственна за различия в предпочтении адгезии, представляя то, что команда назвала кодом адгезии. Этот код был уникальным для каждого из типов клеток и определял, с какими другими клетками каждый тип клеток остается связанным во время морфогенеза.
«Все три молекулы адгезии, которые мы рассмотрели, экспрессируются в разных количествах в каждом типе клеток», – сказал Цай. «Клетки используют этот код для предпочтительного прилипания к клеткам своего собственного типа, что позволяет различным типам клеток разделяться во время формирования паттерна. Но клетки также поддерживают определенный уровень адгезии с другими типами клеток, поскольку они должны сотрудничать, чтобы сформировать ткани. Собирая по кусочкам эти локальные правила взаимодействия, мы можем прояснить глобальную картину ».
Поскольку код адгезии зависит от типа клетки, исследователи предположили, что он, вероятно, контролируется теми же процессами, которые определяют судьбу клетки, а именно передачей сигналов морфогена. Они изучали, как нарушения одного из самых известных морфогенов, Sonic hedgehog (Shh), влияют на тип клеток и соответствующую экспрессию генов молекул адгезии.
Анализ показал, что как тип клеток, так и экспрессия генов молекул адгезии сильно коррелировали как по уровню, так и по пространственному положению. Это справедливо для всего формирующегося спинного мозга, где паттерны экспрессии генов для типа клеток и молекулы адгезии изменяются вместе в ответ на различия в активности Shh.
«Мы обнаружили, что этот морфоген не только контролирует судьбу клеток, но и контролирует клеточную адгезию», – сказал Мегасон. «Модель французского флага дает грубый набросок, а затем дифференциальное сцепление формирует точный рисунок. Сочетание этих различных стратегий, по-видимому, помогает клеткам строить паттерны в трехмерном пространстве и времени по мере формирования эмбриона ».
В настоящее время исследователи продолжают изучать взаимодействие между передачей сигналов морфогенов и адгезией в развивающихся эмбрионах. В текущем исследовании рассматривались только три различных типа клеток, и есть много других кандидатов в молекулы адгезии и морфогенов, которые еще предстоит проанализировать, сказали авторы. Кроме того, детали того, как морфогены контролируют экспрессию как типов клеток, так и молекул адгезии, остаются неясными.
По словам авторов, лучшее понимание этих процессов может помочь ученым раскрыть и реконструировать фундаментальные механизмы, с помощью которых одноклеточное яйцо конструирует целый организм. Это может иметь серьезные последствия для биотехнологии, особенно для усилий по созданию искусственных тканей и органов для трансплантации или для тестирования новых кандидатов в лекарства.
«Проблема тканевой инженерии сейчас заключается в том, что мы просто не знаем, что лежит в основе науки», – сказал Мегасон. «Если вы хотите построить небольшой мост через ручей, возможно, вы сможете сделать это, не разбираясь в физике. Но если вы хотите построить большой подвесной мост, вам нужно много знать о физических принципах. Наша цель – выяснить, каковы эти правила для эмбриона ».
Ссылка: 2 октября 2020 г., Наука.
DOI: 10.1126 / science.aba6637
Дополнительными авторами исследования являются Матеуш Сикора, Пэн Ся, Тугба Колак-Шампольон и Хольгер Кнаут.
Эта работа была поддержана Национальным институтом здравоохранения (гранты R01GM107733, R01NS102322), стипендией K99 Национального института здоровья детей и развития человека Юнис Кеннеди Шрайвер (1K99HD092623), Фондом рака Деймона Руниона, Компанией биологов, Берроуз Фонд Wellcome и Европейский исследовательский совет.