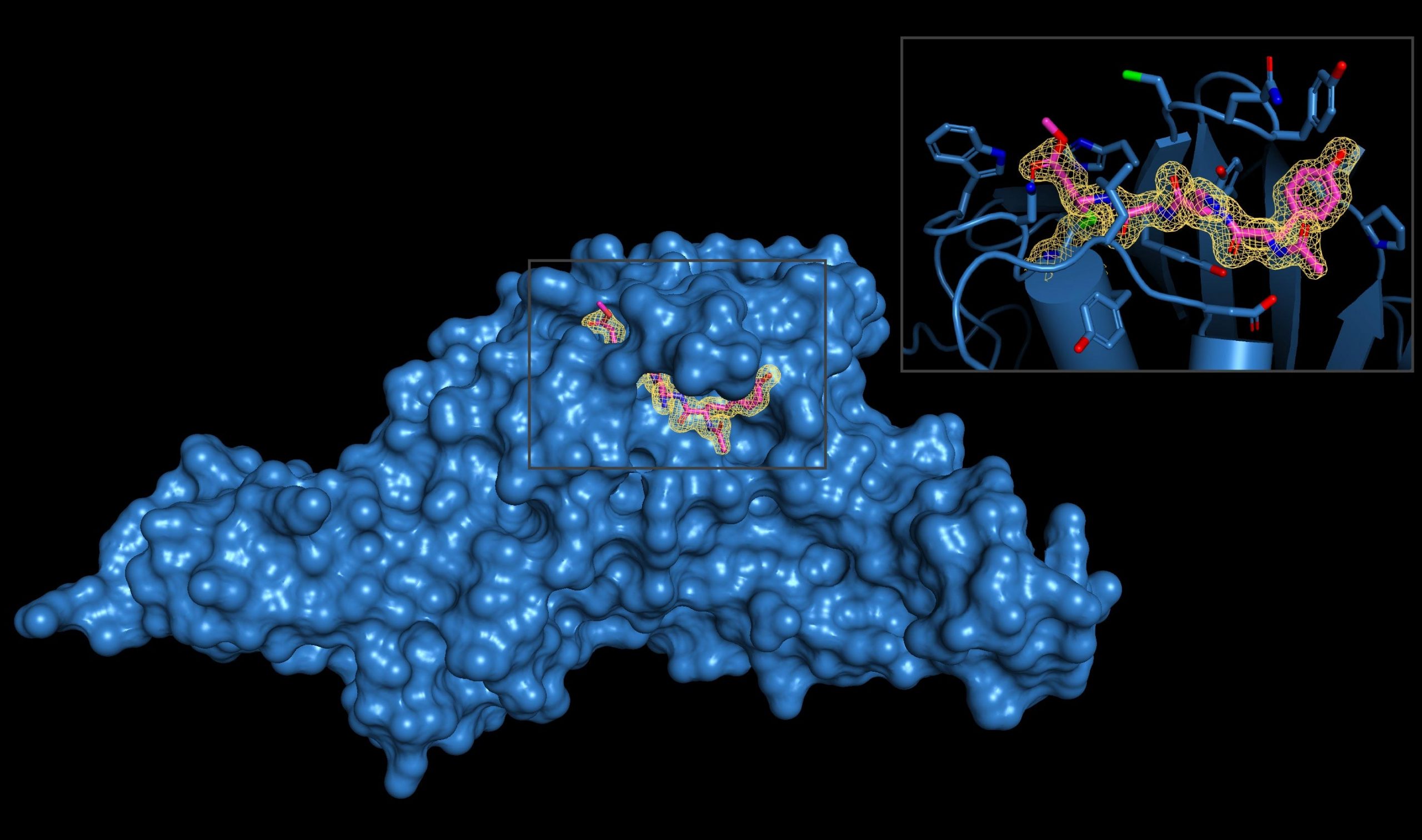
La enzima SARS-CoV-2-PLpro se visualiza con una inserción de la interacción del inhibidor viral. El bloqueo de los efectos de la enzima puede resultar útil para detener las infecciones por coronavirus. Crédito: Imagen cortesía de Shaun K.Olsen, PhD, laboratorio del Centro de Ciencias de la Salud de la Universidad de Texas en San Antonio (Joe R. y Teresa Lozano Long School of Medicine)
El coronavirus utiliza un cortador enzimático para la producción de virus y para desactivar las proteínas inmunes esenciales.
Científicos estadounidenses y polacos, informando el 16 de octubre de 2020 en la revista Avances científicos, expuso un fundamento novedoso para COVID-19 diseño de fármacos: bloqueo de una “tijera” molecular que el virus utiliza para la producción de virus y para desactivar las proteínas humanas cruciales para la respuesta inmunitaria.
Los investigadores son del Centro de Ciencias de la Salud de la Universidad de Texas en San Antonio (UT Health San Antonio) y de la Universidad de Ciencia y Tecnología de Wroclaw. La información recopilada por el equipo estadounidense ayudó a los químicos polacos a desarrollar dos moléculas que inhiben el cortador, una enzima llamada SARS-CoV-2-PLpro.
El SARS-CoV-2-PLpro promueve la infección al detectar y procesar proteínas virales y humanas, dijo el autor principal Shaun K.Olsen, PhD, profesor asociado de bioquímica y biología estructural en la Escuela de Medicina Joe R. y Teresa Lozano Long en UT Salud San Antonio.

Shaun K. Olsen, PhD, estudia la enzima SARS-CoV-2-PL pro y está colaborando con químicos polacos que han desarrollado inhibidores de la enzima. El Dr. Olsen es investigador de la facultad de la Facultad de Medicina Joe R. y Teresa Lozano Long del Centro de Ciencias de la Salud de la Universidad de Texas en San Antonio. Crédito: UT Health San Antonio
“Esta enzima ejecuta un doble golpe”, dijo el Dr. Olsen. “Estimula la liberación de proteínas que son esenciales para que el virus se replique, y también inhibe moléculas llamadas citocinas y quimiocinas que le indican al sistema inmunológico que ataque la infección”, dijo el Dr. Olsen.
El SARS-CoV-2-PLpro corta las proteínas humanas ubiquitina e ISG15, que ayudan a mantener la integridad de las proteínas. “La enzima actúa como una tijera molecular”, dijo el Dr. Olsen. “Escinde la ubiquitina y la ISG15 de otras proteínas, lo que revierte sus efectos normales”.
El equipo del Dr. Olsen, que recientemente se mudó a la Long School of Medicine en UT Health San Antonio de la Medical University of South Carolina, resolvió las estructuras tridimensionales de SARS-CoV-2-PLpro y las dos moléculas inhibidoras, que se denominan VIR250 y VIR251. La cristalografía de rayos X se realizó en el Laboratorio Nacional Argonne cerca de Chicago.
“Nuestro colaborador, el Dr. Marcin Drag, y su equipo desarrollaron los inhibidores, que son muy eficientes para bloquear la actividad del SARS-CoV-2-PLpro, pero no reconocen otras enzimas similares en las células humanas”, dijo el Dr. Olsen. “Este es un punto crítico: el inhibidor es específico para esta enzima viral y no reacciona de forma cruzada con enzimas humanas con una función similar”.
La especificidad será un determinante clave del valor terapéutico en el futuro, dijo.
El equipo estadounidense también comparó el SARS-CoV-2-PLpro con enzimas similares de coronavirus de las últimas décadas, SARS-CoV-1 y MERS. Aprendieron que el SARS-CoV-2-PLpro procesa la ubiquitina y el ISG15 de manera muy diferente a su contraparte del SARS-1.
“Una de las preguntas clave es si eso explica algunas de las diferencias que vemos en la forma en que esos virus afectan a los humanos, si es que afectan”, dijo el Dr. Olsen.
Al comprender las similitudes y diferencias de estas enzimas en varios coronavirus, puede ser posible desarrollar inhibidores que sean efectivos contra múltiples virus, y estos inhibidores podrían modificarse potencialmente cuando surjan otras variantes de coronavirus en el futuro, dijo.
Referencia: “Perfiles de actividad y estructuras cristalinas de proteasa similar a la papaína del SARS-CoV-2 unida a inhibidores: un marco para el diseño de fármacos anti-COVID-19” por Wioletta Rut, Zongyang Lv, Mikolaj Zmudzinski, Stephanie Patchett, Digant Nayak, Scott J. Snipas, Farid El Oualid, Tony T. Huang, Miklos Bekes, Marcin Drag y Shaun K. Olsen, 16 de octubre de 2020, Avances científicos.
DOI: 10.1126 / sciadv.abd4596